CH3COOH là tên gọi hóa học của axit axetic, một axit hữu cơ có công thức phân tử C2H4O2. Axit axetic là một chất lỏng không màu, có mùi đặc trưng của dấm. Axit axetic được sử dụng rộng rãi trong nhiều lĩnh vực như thực phẩm, dược phẩm, hóa chất, nông nghiệp, v.v. Axit axetic cũng là một chất điện li, tức là khi tan trong nước, nó sẽ phân tách thành các ion mang điện tích.
Tuy nhiên, CH3COOH là chất điện li mạnh hay yếu? Đây là câu hỏi mà nhiều người quan tâm, đặc biệt là những người học hoặc làm việc với hóa học.
Trong bài viết này, yukenfucoidan sẽ giải đáp câu hỏi này và giải thích nguyên nhân của nó.
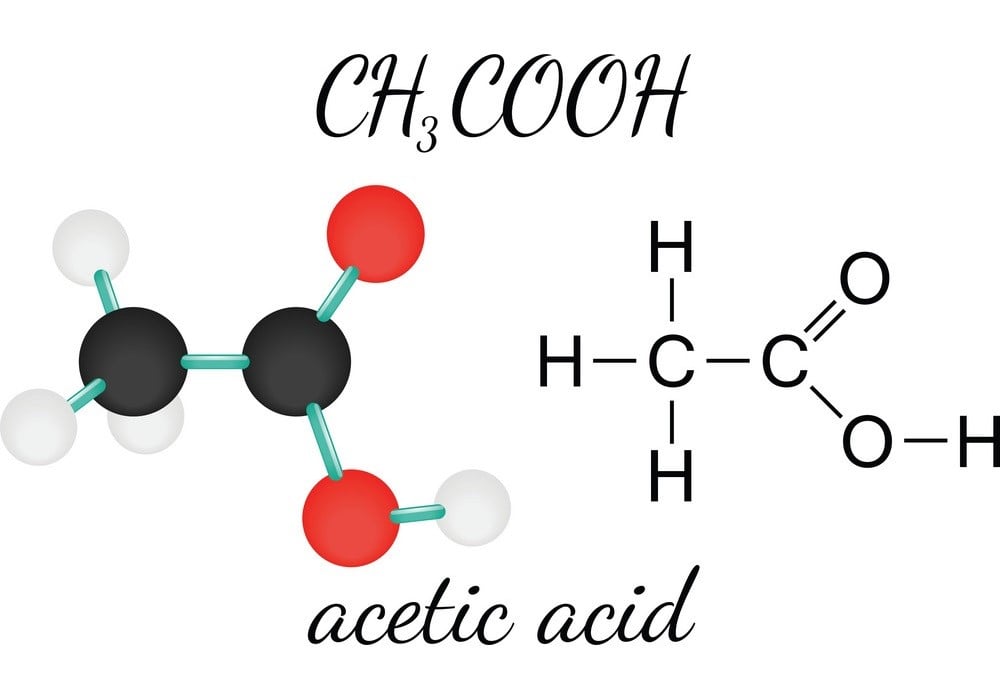
CH3COOH là chất điện li mạnh hay yếu?
Để trả lời câu hỏi CH3COOH là chất điện li mạnh hay yếu, ta cần hiểu khái niệm về chất điện li và các loại chất điện li. Chất điện li là chất khi tan trong nước sẽ phân tách thành các ion mang điện tích khác nhau.
Các ion này có thể dẫn điện trong dung dịch. Có hai loại chất điện li: chất điện li mạnh và chất điện li yếu.

- Chất điện li mạnh là chất khi tan trong nước sẽ phân tách hoàn toàn thành các ion. Ví dụ: NaCl, HCl, NaOH, v.v.
- Chất điện li yếu là chất khi tan trong nước chỉ phân tách một phần nhỏ thành các ion. Phần lớn các phân tử vẫn tồn tại dưới dạng không ion hóa. Ví dụ: CH3COOH, NH3, H2S, v.v.
CH3COOH là chất điện li yếu. Nguyên nhân là vì CH3COOH là một axit yếu, tức là khi tan trong nước, chỉ một phần nhỏ các phân tử CH3COOH sẽ phân li thành ion H+ và ion CH3COO-.
Phần còn lại sẽ tồn tại dưới dạng phân tử không ion hóa.
Phương trình điện li của CH3COOH có thể viết như sau:
CH3COOH ⇌ H+ + CH3COO-
Trong phương trình này, dấu ⇌ biểu thị cho quá trình cân bằng giữa hai chiều phản ứng: chiều thuận (phân li) và chiều ngược (hợp lại).
Nếu ta đo độ dẫn điện của dung dịch CH3COOH, ta sẽ thấy rằng độ dẫn điện rất thấp so với dung dịch của các chất điện li mạnh. Điều này cho thấy rằng chỉ có một lượng nhỏ các ion H+ và CH3COO- được tạo ra trong dung dịch.
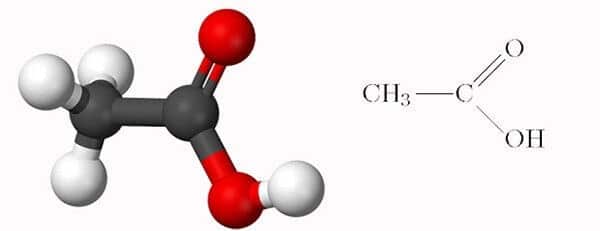
Các yếu tố ảnh hưởng đến độ phân li của CH3COOH
Độ phân li của CH3COOH là chất điện li yếu có thể bị ảnh hưởng bởi một số yếu tố như nồng độ, nhiệt độ, và sự có mặt của các chất khác trong dung dịch. Ta sẽ xem xét từng yếu tố một.
Nồng độ:
Theo nguyên lý Le Chatelier, khi nồng độ của một chất trong dung dịch tăng lên, quá trình phản ứng sẽ diễn ra theo chiều giảm nồng độ của chất đó.
Do đó, khi nồng độ CH3COOH trong dung dịch tăng lên, quá trình phân li sẽ bị giảm đi, và ngược lại. Điều này có nghĩa là dung dịch CH3COOH loãng sẽ có độ phân li cao hơn dung dịch CH3COOH đặc.
Nhiệt độ:
Theo nguyên lý Le Chatelier, khi nhiệt độ của dung dịch tăng lên, quá trình phản ứng sẽ diễn ra theo chiều hấp thụ nhiệt.
Do đó, khi nhiệt độ dung dịch CH3COOH tăng lên, quá trình phân li sẽ được thúc đẩy, và ngược lại. Điều này có nghĩa là dung dịch CH3COOH nóng sẽ có độ phân li cao hơn dung dịch CH3COOH lạnh.
Các chất khác:
Sự có mặt của các chất khác trong dung dịch CH3COOH cũng có thể ảnh hưởng đến độ phân li của nó.
Một số ví dụ cụ thể như sau:
Nếu ta thêm vào dung dịch CH3COOH một lượng nhỏ axit mạnh như HCl hay H2SO4, ta sẽ làm tăng nồng độ ion H+ trong dung dịch.
Theo nguyên lý Le Chatelier, quá trình phân li của CH3COOH sẽ bị ức chế, do chiều ngược (hợp lại) được ưu tiên. Điều này có nghĩa là dung dịch CH3COOH sẽ có độ phân li thấp hơn khi có axit mạnh.
Nếu ta thêm vào dung dịch CH3COOH một lượng nhỏ bazơ mạnh như NaOH hay KOH, ta sẽ làm giảm nồng độ ion H+ trong dung dịch.
Theo nguyên lý Le Chatelier, quá trình phân li của CH3COOH sẽ được kích thích, do chiều thuận (phân li) được ưu tiên. Điều này có nghĩa là dung dịch CH3COOH sẽ có độ phân li cao hơn khi có bazơ mạnh.
Nếu ta thêm vào dung dịch CH3COOH một lượng nhỏ muối của axit yếu và bazơ mạnh như NaCH3COO hay KCH3COO, ta sẽ làm tăng nồng độ ion CH3COO- trong dung dịch.
Theo nguyên lý Le Chatelier, quá trình phân li của CH3COOH sẽ bị ức chế, do chiều ngược (hợp lại) được ưu tiên. Điều này có nghĩa là dung dịch CH3COOH sẽ có độ phân li thấp hơn khi có muối.
Làm thế nào để tăng độ phân li của CH3COOH?
Để tăng độ phân li của CH3COOH, bạn có thể thực hiện một số cách sau:
- Giảm nồng độ CH3COOH trong dung dịch bằng cách pha loãng nó với nước. Điều này sẽ làm giảm sự ức chế của quá trình phân li và tăng độ phân li của CH3COOH.
- Tăng nhiệt độ dung dịch CH3COOH bằng cách đun nóng nó. Điều này sẽ làm tăng sự kích thích của quá trình phân li và tăng độ phân li của CH3COOH.
- Thêm vào dung dịch CH3COOH một lượng nhỏ bazơ mạnh như NaOH hay KOH. Điều này sẽ làm giảm nồng độ ion H+ trong dung dịch và tăng độ phân li của CH3COOH.
Trong bài viết này, yukenfucoidan đã giải đáp câu hỏi CH3COOH là chất điện li mạnh hay yếu và giải thích nguyên nhân của nó. Hi vọng bài viết này hữu ích với bạn.


